K. JAWAD, A. BENNANI, Kh. LAHLOU
Service d'odontologie conservatrice
Faculté de médecine dentaire de Casablanca - Maroc
Université Hassan II
RÉSUMÉ
La biocompatibilité pulpaire des adhésifs et des résines composites est fonction de la nature et de la stabilité chimique des matériaux après polymérisation, ainsi que de l'étanchéité des restaurations réalisées.
Dans l'idéal, les matériaux ne devraient contenir aucun composant cytotoxique. Leurs potentiels de dissolution, diffusion -et dégradation devraient être négligeables et leur adhérence aux tissus dentaires telle, qu'ils puissent s'opposer aux micro-infiltrations marginales.
Par rapport aux matériaux plus anciens, la biocompatibilité pulpaire des adhésifs et composites dentaires actuels s'est nettement améliorée. Cette amélioration est directement liée à la capacité élevée d'adhérence et à l'étanchéité de ces matériaux.
Mots-clés : Système adhésif, Résine composite, Adhérence, Etanchéité, Biocompatibilité, dentinaire, dentinopulpaire.
Le collage de matériaux restaurateurs doit simultanément restaurer l'esthétique et la fonction et prévenir la réinfection des tissus dentaires et pulpaires sous-jacents.
Leur innocuité vis-à-vis des tissus pulpaires doit permettre à la pulpe de conserver ou de retrouver durablement un état de santé physiologique.
Idéalement, tout matériau dentaire utilisé dans la cavité buccale devrait :
- Ne présenter aucun danger pour la pulpe et les tissus mous environnants.
- Ne contenir aucune substance toxique diffusible susceptible d'être absorbée par vole sanguine et de créer une réponse toxique systémique.
- Ne pas être un agent de sensibilisation et induire une réponse allergique.
- Ne pas être carcinogène.
Si certains des matériaux de restauration sont relativement inertes (or, céramique), et intrinsèquement peu dangereux, les matériaux plastiques esthétiques (adhésifs, composites, verres ionomères) qui contiennent des composites chimiquement réactifs peuvent exercer des effets nocifs sur la pulpe et les tissus muqueux adjacents.
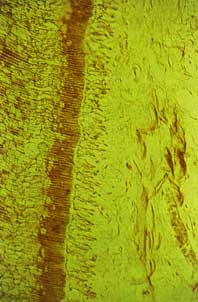 |
LE COMPLEXE DENTINOPULPAIRE SUBSTRAT VIVANT
La pulpe est un tissu conjonctif spécialisé, sensible aux agressions, emprisonné sous une coque rigide de dentine et d'émail. Elle répond aux stimulations physiologiques et pathologiques d'une façon univoque.
La dentine est parcourue par les tubuli dentinaires qui renferment un prolongement odontoblastique, du collagène, des fluides et éventuellement des nerfs non myélinisés. La relation étroite des deux tissus nous mène à ne pas les séparer et à parler du complexe dentino-pulpaire (1).
La défense de l'organe pulpo-dentinaire s'organise sur plusieurs lignes et sur plusieurs périodes de temps. Certains de ces mécanismes se déroulent dans la dentine, d'autres au niveau de la pulpe (2,3) (Fig. 1).
La douleur dentinaire :
Signe que les tubuli dentinaires sont ouverts et communiquent avec l'extérieur à la suite d'une lésion carieuse, d'une fracture ou d'une érosion. Il s'agit d'un système d'alarme (4).
Les phénomènes constructifs :
La sclérodentine :
Est une dentine hyperminéralisée qui conduit à l'oblitération des canalicules et s'oppose ainsi à la pénétration de l'agent irritatif vers la pulpe et de réduire fortement les mouvements de fluide dans la dentine. C'est la première ligne de défense du complexe dentino-pulpaire (2, 3, 4), elle se produit par précipitation de gros cristaux isodiamétriques de whitlockite dans la lumière tubulaire et par une hypertrophie de la dentine péritubulaire (5).
La dentine tertiaire :
Elle représente la deuxième ligne de défense. C'est une réaction retardée et lente, qui ne peut supprimer sur le champ la pénétration des irritants (2). En fonction de l'intensité de l'agression et du potentiel réparateur propre à la dent, elle représente un aspect histologique variable allant de l'orthodentine tubulaire bien structurée à une fibrodentine plus ou moins anarchique (3).
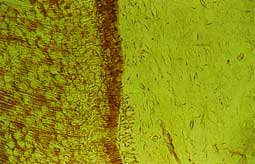
Les réactions pulpaires inflammatoires :
Il est admis que la réaction inflammatoire se déclenche dans la pulpe dès que la concentration d'un irritant dépasse un certain seuil. Ce seuil franchi, les moyens de défense de l'organisme tout entier sont mobilisés. En dessous de ce seuil, la défense et la protection du tissu pulpaire sont assurées par la barrière dentinaire principalement et particulièrement grâce aux divers mécanismes et réactions qui diminuent sa perméabilité (2).
L'inflammation initiale est donc caractérisée par des phénomènes essentiellement vasculaires avec présence de cellules inflammatoires et est encore réversible. Les étapes suivantes, pulpite séreuse puis abcédente, aboutissent à la nécrose de la pulpe (Fig. 2, 3a, 3b).
 |
 |
 |
|
LES ADHÉSIFS AMELO-DENTINAIRES
Depuis leur avènement, les adhésifs ont connu une évolution très importante. Ceux qui adhèrent directement à la boue dentinaire sans l'utilisation d'un primer acide, et ceux qui utilisent un primer acide pour altérer la boue dentinaire avant ou pendant le collage (6).
Les adhésifs dentinaires de première génération :
Introduite dans les années 60, la première génération d'adhésifs ne développait qu'un faible collage chimique avec le calcium de la partie inorganique de la dentine. Basée sur le NPG-GMA, leur force d'adhésion limitée à 2,5 MPa se révélera insuffisante pour annuler la force de rétraction due à là polymérisation des résines composites, évaluée à 17 -20 MPa (7).
Cette génération ne prend pas en compte le problème de la boue dentinaire. Elle s'intéresse plus à la biocompatibilité vis-à-vis du complexe dentino-pulpaire (8) en diminuant la perméabilité des canalicules dentinaires.
Parmi ces adhésifs, on trouve : le Pertac et le Prisma universal Bond 2 (Fig. 4).
Les adhésifs dentinaires de deuxième génération :
Au début des années 80, les adhésifs de la deuxième génération agissaient sur une dentine pré-traitée à l'aide de EDTA à 0,22%, et réalisaient un collage chimique avec les parties organiques et inorganiques de la dentine (7).
La boue dentinaire était perçue comme un barrage à la diffusion des agressions en direction pulpaire et le principe de cette génération consiste à imprégner la boue dentinaire sans l'ôter (8).
Cependant, cette dernière ne peut être considérée comme une barrière fiable puisqu'elle n'est qu'un magma de débris dentinaires nécrosés, des bactéries et des produits organiques.
L'adhésion est améliorée mais reste limitée: la solution acide, trop faible, n'élimine que la partie la plus superficielle de la boue dentinaire sans atteindre la surface dentinaire sous-jacente (Fig. 5).
Les adhésifs dentinaires de troisième génération :
A la fin des années 80, les adhésifs de troisième génération ouvrent la voie d'un collage véritable avec la dentine, à la fois chimique et micromécanique. Bon nombre d'adhésifs commercialisés aujourd'hui font encore appel à ce système d'adhésion.
Le principe de ces adhésifs consiste à éliminer la boue dentinaire en faisant subsister le bouchon et la dentine péricanaliculaire dans le but d'éviter les lésions pulpaires, susceptibles d'être induites par des solutions acides trop concentrées et de dresser un barrage contre l'infiltration bactérienne qui pourrait survenir par l'intermédiaire des portes d'entrée canaliculaires.
Pour ce faire, des acides de faible concentration sont utilisés (acide maléique 2,5%, du scotchbond 2 -(3M) et EDTA à 17% du Gluma (Bayer).
Dans ces systèmes, la présence d'un primer d'adhésion, constitué de HEMA permet d'augmenter la mouillabilité du substrat dentinaire et de faciliter la pénétration de la résine liquide. Avec ces adhésifs, on parvient à obtenir des valeurs d'adhésion à la dentine de 8 à 11 MPa, bien supérieures aux valeurs obtenues avec les adhésifs des deux premières générations mais insuffisantes pour s'opposer aux formes de contraction (7, 8) (Fig. 6).
 |
 |
 |
 |
 |
|
Les adhésifs de quatrième génération :
C'est actuellement l'approche qui permet d'obtenir les valeurs d'adhésion les plus élevées associées à une bonne étanchéité.
Un contact intime avec la dentine ne peut être obtenu que si la couche de boue dentinaire est entièrement dissoute et incorporée à la couche d'adhésif ou totalement éliminée. C'est deux résultats peuvent être obtenus par traitement avec des solutions acides. L'obtention d'une couche déminéralisée d'environ 3 à 10 mm dépend du type et de la concentration de l'acide ainsi que de la durée du mordançage. L'interaction des acides avec la dentine est limitée par l'effet tampon de l'hydroxyapatite. Le mordançage non seulement dissout la boue dentinaire, mais élimine pareillement la couche superficielle de dentine, ouvre les tubules, leur donne une forme d'entonnoir et déminéralise la surface.
Après le mordançage de la dentine et le rinçage des parois de la cavité, la dentine déminéralisée est réduite à une trame de collagène car le support d'hydroxyapatite a disparu. Cette couche riche en collagène a un niveau d'énergie de surface bas. Les espaces interfibrillaires de 15 à 20 nm précédemment remplis d'hydroxyapatite contiennent maintenant de l'eau. Cette eau doit être remplacée par le monomère. Tout séchage de la dentine provoque une perte d'eau avec un affaissement des fibres de collagène qui gêne la pénétration des monomères dans la dentine déminéralisée. Il est donc recommandé de garder la dentine déminéralisée humide ou moite.
L'infiltration dans le collagène aboutit à la formation d'une couche mixte appelée "couche hybride" ou " zone d'interdiffusion résine-dentine".
Le processus d'action du primer est d'humidifier les fibrilles de collagène exposées, en éliminant l'humidité de surface résiduelle, en transformant une surface hydrophile en surface hydrophobe, et en faisant pénétrer suffisamment le monomère dans les espaces interfibrillaires de la dentine déminéralisée. Pour cela, il est combiné avec un solvant comme l'acétone et/ou l'éthanol, qui aident au déplacement de l'eau du réseau de collagène humide (9, 10) (Fig. 7).
Les adhésifs de cinquième génération:
Ces dernières années, quelques modifications de la technique et quelques changements structurels des adhésifs de quatrième génération ont donné naissance à ceux de la cinquième génération.
Dans le but de simplifier la tâche du praticien, les fabricants ont réuni les étapes du mordançage acide et du primer qui ne nécessite pas de rinçage, ou celle du primer et du bonding.
Les adhésifs du 51, génération sont plus rapides, plus ergonomiques et aussi adhérents que les adhésifs de 4ème génération (11).
Plusieurs études ont prouvé que les adhésifs multi-séquentiels en combinaison avec la technique de mordançage total sont d'une efficacité plutôt constante pour ce qui concerne la résistance du collage ou l'adaptation des bords, alors que les adhésifs monocomposants ne sont pas aussi performants (9).
Biocompatibilité des systèmes adhésifs sur la dentine des dents pulpées :
A la fin des années 30, des publications commencèrent à rapporter qu'un pH bas était le principal facteur d'inflammation pulpaire (Manely) (1).
jusqu'à la fin des années 70, cette opinion était partagée par beaucoup de chercheurs (Brouillet, Francquin, Langeland) (1).
Depuis la fin des années 1980, Bergenholtz et Lindhe (1) ont montré que l'infection des tissus dentaires (carie, et pulpopathies) est simplement la conséquence de l'infection bactérienne et n'a rien à voir avec le PH d'un matériau.
D'après l'étude de Snuggs et coll (1993), le coiffage pulpaire direct avec un adhésif de 411, génération est couronné de succès mais seulement en l'absence d'infection bactérienne. De plus la formation de ponts dentinaires après l'application de résines adhésives sur des pulpes exposées a été histologiquement démontrée.
Cox et Suzuki (1994) ont démontré que les bases et les fonds de cavités à l'hydroxyde de calcium ne procurent pas une protection à long terme contre les infiltrations bactériennes car elles n'adhèrent pas à la dentine vivante (1).
Katoh (2000) indique que chez l'homme la cicatrisation, est bonne lorsque l'adhésif dentinaire est utilisé pour les coiffages pulpaires directs, bien que la cicatrisation soit légèrement plus rapide avec l'hydroxyde de calcium. Il conseille d'appliquer l'hydroxyde de calcium sur l'effraction, puis de recouvrir celui-ci ainsi que la dentine profonde périphérique avec de la résine qui sera hybridée (2).
Une variable non négligeable est le contrôle du saignement. Il existe plusieurs options thérapeutiques : l'une d'elle consiste à traiter l'effraction pulpaire avec de l'hypochlorite de sodium à 5% pendant 2 min pour éliminer le caillot sanguin et nettoyer le site exposé, l'autre consiste à rincer avec du sérum, de la lidocaïne 2% adrénalinée ou une solution d'hydroxyde de calcium jusqu'à ce que le saignement s'arrête.
La nature du matériau placé sur la plaie n'est pas aussi importante que le scellement périphérique et la réduction de l'hémorragie (2).
Pour conclure, les données actuelles démontrent indubitablement l'innocuité biologique de divers traitements de mordançage acide sur dents humaines dans le cadre de traitements restaurateurs définitifs (1).
LES RÉSINES COMPOSITES
Les résines composites sont apparues en dentisterie dans le milieu des années 60. Depuis, leur développement a été énorme. Les composites les plus utilisés aujourd'hui sont photopolymérisables, matériaux monocomposants constitués de trois éléments :
- Une résine à base de monomères du méthacrylate relativement hydrophobe et contenant un initiateur de polymérisation,
- Des charges inorganiques faites de particules de verre, de quartz et/ou de silice vitreuse,
- Un agent de couplage qui lie chimiquement les charges à la matrice de résine.
Classification des composites :
Les composites chémopolymérisables :
Les premiers composites apparus sur le marché, à l'aube des années 70, étaient chémopolymérisables. Ils se présentaient sous une forme pâte-pâte. Leur malaxage entraînait l'inclusion de bulles, qui nuisaient tant à l'esthétique qu'à la résistance du matériau. Par ailleurs, ces composites traditionnels avaient des charges de taille et de répartition grossières, d'où un polissage difficile et des performances qui limitaient leur usage au secteur antérieur.
Les composites photopolymérisables ont constitué une véritable innovation. L'absence de spatulation évite l'incorporation de bulles lors du mélange. Le praticien dispose d'une entière liberté sur le temps de prise. Il peut multiplier les apports et modeler le matériau à souhait.
Les composites chémopolymérisables conservent quelques indications, comme les reconstitutions de faux-moignons sur dents dépulpées (11) et comme base intermédiaire (substitut dentinaire) sur dents pulpées.
Les composites hybrides :
Le début des années 80 a vu l'introduction des composites dits "hybrides", destinés à se substituer à l'amalgame pour les restaurations postérieures. La dénomination "d'hybrides" indique qu'ils contiennent deux types de charges :
- Des charges de verres dont la taille est comprise entre 1 et 30 micromètres,
- Des microcharges de silice colloïdale (0,04 micromètres).
Malheureusement, ces matériaux se sont révélés peu résistants à l'usure en comparaison de l'amalgame (11).
Les composites micro-hybrides :
Pour palier les médiocres performances des composites hybrides dans le secteur postérieur et pour améliorer leur aspect, des composites micro-hybrides ont été développés au début des années 90.
Le diamètre des charges de verre est réduit. Il est dans une fourchette de 0, 1 à 3 micromètres. Une judicieuse répartition granulométrique a permis d'augmenter le taux de charges, conduisant à des matériaux plus denses. La géométrie des charges a également évolué : elle est plus douce afin de limiter les zones de concentration de contraintes au sein du matériau.
Ces modifications procurent une résistance à l'usure proche de celle de l'amalgame.
Par ailleurs, la taille réduite des charges, dans des dimensions proches de celle du spectre de la lumière, permet un aspect esthétique très satisfaisant, avec une meilleure aptitude au polissage.
Ce sont des composites universels : antérieurs et postérieurs (11).
Les composites micro-hybrides compactables :
Différents moyens permettent de moduler la consistance des composites microhybrides afin de les rendre compactables. Nous citons ici deux exemples parmi d'autres.
Le P60 (3 M Santé) reprend le même type de charges que le ZIOO. Sa matrice est à base de monomères de haut poids moléculaire qui donnent à ce composite un caractère compactable. Il est indiqué pour des restaurations postérieures.
Dans le Prodigy Condensable® (Kerr), les charges sont recouvertes d'un tensioactif qui permet l'incorporation d'un plus grand volume de charges et donc d'augmenter la viscosité (meilleure compacité). Le retrait de polymérisation est donc réduit.
La matrice comprend un agent de couplage matrice-charge, destiné à relaxer les contraintes de polymérisation.
Ces particularités modifient les propriétés rhéologiques et rendent le matériau compactable (11).
Les composites micro-hybrides fluides :
La matière et les charges sont identiques à celles des micro-hybrides classiques. Les charges sont en plus faible quantité : environ 60% en poids (40% en volume). Ceci réduit le module d'élasticité de ces composites et les rendrait capables de mieux absorber les contraintes (mastication, polymérisation).
Malheureusement, cette diminution du taux de charges augmente considérablement le retrait de polymérisation (11).
Dernières évolutions des composites micro-hybrides :
Plus d'esthétique et moins de retrait.
Les gammes de teintes et d'opacités sont élargies pour permettre un montage élaboré de la restauration.
L'Esthet X (Densply) fait partie des nouveaux composites destinés à être montés par stratification pour un haut rendu esthétique. La matrice est identique à celle de son prédécesseur (Prisma TPH, Dentsply). Par contre, les charges sont principalement constituées de verre de baryum, afin d'optimiser les propriétés esthétiques. La distribution des diamètres des charges est celle d'un composite micro-hybride classique (de 0,02 à 3 micromètres). Des micro particules de silice de quelques nanomètres complètent les charges de baryum, afin d'augmenter l'aptitude au polissage.
L'Enamel HFO (Bisico) est également un composite micro-hybride à haut rendu esthétique.
Le Point 4 (Kerr) a des charges ne dépassant pas 1 micromètre. Ce composite représente, avec l'Enamel HFO (Bisico), une nouvelle tendance vers la réduction de la taille des charges et de la distribution des diamètres. Il est encore trop tôt pour savoir quel est le comportement à l'usure de ce type de composites (11).
Propriétés biologiques :
Effet cariostatique :
Les nouvelles résines composites peuvent acquérir un pouvoir cariostatique par l'incorporation de dérivés fluorés sous forme de charges minérales susceptibles de relayer des ions fluor ou sous forme de monomères fluorés (octofluoro-pentyl méthacrylate) copolymérisés avec la résine matricielle.
Les applications potentielles sont l'amélioration du comportement à long terme des restaurations en composite, les collages en orthodontie, les fonds de cavité photopolymérisables et le scellement de puits et fissures.
Cependant, la libération de fluorures par les résines composites est faible et limitée dans le temps si on les compare avec les verres inomoères conventionnels ou hybrides ainsi que les compomères (12).
Toxicité directe :
Ce sont essentiellement les différents constituants de la résine monomère qui sont responsables des effets secondaires potentiels des composites, et en particulier des risques de carcinogénicité et de cytotoxicité locale.
Ces risques existent mais les accidents dus aux composites sont rares, et peuvent être évités ou minimisés par une sélection pertinente et un usage clinique rigoureux des matériaux.
De plus, la cytotoxicité intrinsèque des matériaux adhésifs est liée à leur stabilité chimique après polymérisation.
Le risque de dégradation et de libération de composants toxiques augmente avec l'insuffisance de polymérisation. Ces monomères libres (HEMA, MMA) sont solubles dans l'eau et ont un faible poids moléculaire. Ils pourront diffuser au travers des canalicules en direction pulpaire, mais ce problème est résolu par la couche hybride (12).
Toxicité indirecte :
Pour la majorité des auteurs, la pénétration des bactéries au niveau de l'interface matériau/dent relative avec l'absence ou la perte d'étanchéité des restaurations est le facteur essentiel d'irritation pulpaire.
Lorsque le décollement intervient, les contraintes thermiques et mécaniques sur la restauration peuvent exercer un effet de pompage sur les fluides dentinaires occupant le hiatus le long de la paroi cavitaire, et probablement chasser les irritants et les toxines bactériennes dans les canalicules (12).
Biocompatibilité :
La nocivité des résines composites peut se manifester par l'apparition de dentine réactionnelle, une inflammation pulpaire, ou une dégénérescence pulpaire. Cox ne trouve pas de corrélation entre l'épaisseur de dentine réparatrice et les matériaux de restauration utilisés. Par contre, l'épaisseur de dentine réactionnelle varie quand la préparation de la cavité s'effectue dans le tiers interne de la dentine. L'épaisseur résiduelle de dentine détermine l'intensité des réactions pulpaires. Mais cette production de dentine réactionnelle est plus liée aux microtraumatismes durant la préparation qu'à la toxicité du matériau (12).
Tolérance parodontale :
Elle est liée à l'état de surface du matériau et à la qualité de l'interface dent-matériau au niveau cervical, qui n'est pas immédiatement stabilisée puisque le composite subit des contraintes durant la polymérisation.
Afin de limiter la rétention de plaque bactérienne, le matériau doit être parfaitement poli, ce qui est plus facile avec les hybrides récents. Des études ont mis en évidence la colonisation bactérienne des surfaces rugueuses, ainsi que la difficulté à obtenir la même qualité de polissage sur toutes les zones de la restauration. Par ailleurs, il semble que pour un même état de surface, les bactéries n'adhèrent pas de façon identique sur tous les composites.
Les cavités sous-gingivales sont donc déconseillées, d'autant que toute préparation débordant sur les zones radiculaires est aléatoire : adhésion précaire, finitions difficiles et imparfaites.
La règle est donc de se tenir à distance des tissus parodontaux, ce qui peut être obtenu dans certains cas par le recours à une préparation chirurgicale préalable (13).
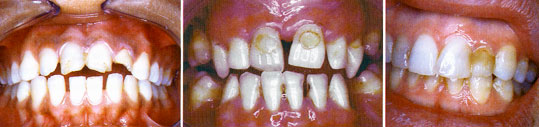
lnfluence du praticien :
La perte d'herméticité (fig. 8, 9, 10) peut être inhérente à des erreurs du praticien et à sa technique d'obturation :
- Un défaut d'isolation du champ opératoire peut entraîner une contamination par la salive et/ou le sang.
- L'huile en provenance des instruments rotatifs peut aussi altérer la qualité du collage.
- Une adaptation insuffisante du composite dans sa cavité, ainsi qu'un non respect des protocoles opératoires sont de grandes sources d'échec.
- Le retrait des résidus de ciment contenant de l'eugénol est primordial.
Ainsi, on préconise une obturation temporaire au verre inonomère lorsqu'on souhaite différer une obturation adhésive (8).
 |
Conseils d'utilisation des composites compactables :
Point de contact :
Les composites compactables ont une consistance qui permet de les condenser, avec un fouloir à bout lisse, de façon similaire à un amalgame. Cette propriété ne suffit pas, à elle seule, à garantir un point de contact proximal correct. Il est nécessaire d'utiliser un écarteur et de plaquer la matrice contre la dent adjacente avec un fouloir, au moment de la polymérisation (11).
Epaisseur de chaque couche de composite :
Les composites compactables ont un plus faible retrait de polymérisation que ceux des composites micro-hybrides classiques. Il est donc tentant d'augmenter la quantité de matériau mise en place à chaque apport. En effet, une étude réalisée par Gonthier et coll. en 2000 sur l'étanchéité des obturations des cavités classe V, a prouvé que les composites compactables assurent la même étanchéité d'obturation en un seul apport que les composites micro-hybrides classiques en deux apports (11).
Adaptation des composites compactables aux parois cavitaires :
La viscosité plus importante des composites compactables réduit leur mouillabilité, c'est à dire leur aptitude à s'étaler sur les parois de la cavité. Il faut alors effectuer une condensation énergique et prolongée qui risque d'incorporer des bulles dans le matériau. Un autre technique consiste à appliquer, sur les parois, une base de composite de faible viscosité (composites dits fluides) et recouvrir ensuite par le composite compactable.
Les résultats montrent que l'application d'un composite fluide augmente significativement l'étanchéité des obturations, à condition que ce composite soit photopolymérisé en même temps que le composite micro-hybride (11).
CONCLUSION
L'utilisation raisonnée d'un agent acide sur la dentine des dents pulpées, suivie de son scellement étanche à l'aide de promoteurs d'adhésion hydrophiles et d'agents de liaison viscoélastiques représente en terme de biocompatibilité pulpaire la solution clinique actuelle la plus acceptable.
En effet, le succès clinique dépend plus de la technique d'application et la manipulation correctes que du produit lui même.
BIBLIOGRAPHIE
1- Cox E Charles. Interaction des résines adhésives avec les tissus dentaires vivants. Réal. Clin., 1994, 5 (4) :411-420.
2- Ciuchi B., Bouillaguet S., Holz J. La perméabilité dentinaire et ses implications cliniques. Réal. Clin., 1995, 6 (2) : 145-157.
3- Lessous J., Mathiew R., Brouillet J.L. Thérapeutique pulpo-dentinaire : les différentes possibilités de coiffage. Rev. Fr. Endo., 1986, 5 (1) : 73-88.
4- FabiotT Odontologie conservatrice. Atlas Pratique, Paris SNPMD, 1985 : 90-12 1.
S-Triller M. Histologie dentaire. Masson, Ed., Paris, 1986.
6- Vannoort R. Principes de base de l'adhésion en dentisterie. Rev. Odonto-Stomatol, 1995, 24 (4) : 257-27 1.
7- Gorracci G., Mari G. Les bases adhésives de la dentisterie conservatrice esthétique. Réal. Clin., 1998, 9 (3) : 295-312.
B- Lugand P., Colon P Etude rationnelle des systèmes adhésifs commercialisés. Réal. Clin., 1994, 5 (4) : 529-538.
9- Roulet J.F, Degrange M. Collage et adhésion. Berlin-Paris, 2000 : 29-42.
10- Lamibrechts P., Meerbeek B.V., Perdigâo J.,Vanherle G. Le collage : ce qu'on doit faire, ce qu'on ne doit pas faire. Collage et adhésion, Berlin-Paris, 2000 : 29-42.
11 - Gonthier S., Sitbon K., Degrange M. Composites compactables et fluides : quels apports pour la pratique quotidienne ?. Clinic, 2000, 21 (6) 399-406.
12- Lasfargues J.J., Goldsberg M. Biocompatibilité pulpaire des adhésifs et résines composites de dernière génération. Réal. Clin., 1994,5 (4) :421-437.
13- Roth E Le collage amélo-dentinaire. Chir. Dent. Fr., 1992, 600 :3 1-44.








