Publié le 09-07-2013
S. BOUZOUBAA, I. BENYAHYA
Service d’odontologie chirurgicale - CCTD de Casablanca
Faculté de médecine dentaire de Casablanca
Université Hassan II
RÉSUMÉ
Le lichen plan (LP) est une maladie inflammatoire d’évolution chronique et récidivante, généralement bénigne, atteignant la peau, les phanères et les muqueuses malpighiennes (1). L’origine exacte du LP est mal connue.
Le diagnostic positif se base sur les éléments cliniques et surtout anatomopathologiques.
Histologiquement, on trouve un infiltrat lymphocytaire en bande du derme superficiel associé à une nécrose kératinocytaire des couches basales.
Les formes cliniques sont multiples et la symptomatologie est variée.
La transformation maligne du LPB reste un sujet de controverses malgré les nombreuses études qui lui ont été consacrées.
Mots clés : Lichen plan buccal, lésion lichénoïde, lichen plan cutané, hépatite «C», transformation maligne.
INTRODUCTION
Le lichen plan buccal reste d’étiologie incertaine, Il atteint de façon prépondérante les femmes d’âge moyen (quatrième et cinquième décennies). Sa découverte par un médecin dentiste averti permet une prise en charge précoce ou même un dépistage de pathologies générales associées (1).
ÉPIDÉMIOLOGIE
ÉTIOPATHOGÉNIE
FACTEURS ÉTIOLOGIQUES
LPB et maladies associées
En France, une étude rétrospective entre 1992 et 1996 sur 28 patients présentant un lichen plan oral a révélé que 8 patients soit (29%) étaient positifs aux anticorps anti-VHC.L’apparition ou l’aggravation du LP sous interféron au cours d’une hépatite chronique C a également été décrite (4-10).
Au Maroc, une étude réalisée en 2001 sur 19 patients avec un LPB a montré que 9 patients soit (45,5%) présentaient une association LPB et HVC. Dans (21%) des cas le LPB a permis le dépistage de la pathologie (11).
L’association diabète et LPB est controversée, alors que l’association papillomavirus et LPB a été signalée (HPV 16, 18) avec une importante fréquence (2).
Réaction du greffon contre l’hôte
La prise médicamenteuse
Le matériel dentaire
En 2003 THORNHILL et coll. constatent une amélioration chez 93% de patients présentant des lésions lichénoides en rapport avec l’amalgame après remplacement de ce dernier par du composite (13).
Facteurs neurologiques et psychosomatiques
Habitudes de vie
Ils sont considérés comme des facteurs carcinogènes favorisant la transformation maligne d’un LPB déjà présent (2).
FORMES CLINIQUES (2,3)
Forme en réseau
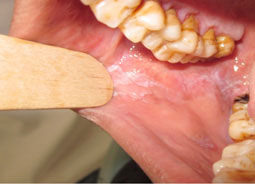
Forme érosive
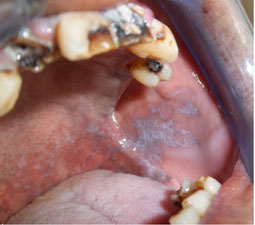
La forme érosive, douloureuse, présente un aspect rouge vif vernissé, au fond oedématié, de taille variable et légèrement en saillie. Ce sont des érosions à limites nettes des gencives, de la face dorsale et des bords latéraux de la langue. Le phénomène de Koebner est constaté au niveau muqueux (Fig.2).
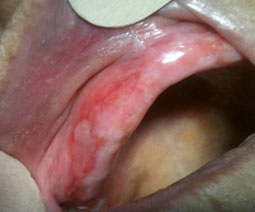
Forme atrophique
C’est une forme d’évolution d’un lichen plan ancien. L’aspect est lisse et légèrement déprimé. L’atrophie se traduit par des plages dépapillées, ainsi par une diminution du fond du vestibule et de l’ouverture buccale (Fig.3).
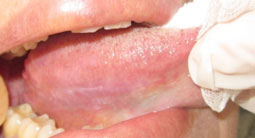
Forme bulleuse
Elle précède la forme érosive; le toit de la bulle est alors quelques fois retrouvé en périphérie (Fig.4).
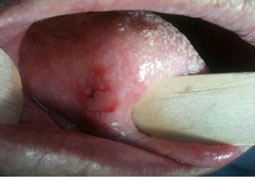
Forme nigricans
Elle se présente avec des pigmentations brunâtres ou noirâtres, mal limitées et post-inflammatoires (Fig.5).

DIAGNOSTIC
Anamnèse
Au cours de l’anamnèse, les antécédents personnels et familiaux, ainsi que les médicaments absorbés sont des éléments importants à relever et qui peuvent orienter vers un diagnostic étiologique précis. L’interrogatoire permet également d’évaluer non seulement l’état général du patient mais également les habitudes de vie et la présence ou pas d’une composante anxieuse.
Examen clinique
Sur le plan cutané, l’examen clinique doit s’intéresser à la face antérieure des poignets, des avant-bras, des jambes et du dos qui constituent les zones cutanées de prédilection du LP cutané.
L’examen endobuccal doit comprendre la totalité de la muqueuse buccale ainsi que la qualité des restaurations et des prothèses, leurs situations par rapport aux lésions.
Examen paraclinique
L’examen anatomopathologique est l’examen fondamental qui permet de confirmer le diagnostic de lichen plan buccal et analyser son activité. Trois éléments anatomopathologiques conduisent à ce diagnostic : l’hyperkératose ou la parakératose, la dégénérescence du stratum germinatum et l’infiltrat lymphocytaire en bande sous épithéliale (14).
DIAGNOSTIC DIFFÉRENTIEL
Il est classique de distinguer le lichen plan buccal des réactions lichénoïdes médicamenteuses, aux amalgames dentaires et celles de la réaction du greffon contre l’hôte en sachant que les limites de ces entités sont parfois difficiles à définir (2).
TRANSFORMATION MALIGNE DU LPB
La World Health Organization (WHO) en 2005 a remplacé le terme de précancéreux ou pré-malin par le terme de potentiellement malin. Dans la littérature, il est discuté du risque augmenté de développement de carcinome spinocellulaire sur un LP pré-existant mais cette question n’est pas formellement résolue. Cependant, le LB est accepté comme un état à potentiel malin.
Gandolfo et coll a montré dans une étude faite sur 402 patients que le risque de développer un carcinome spinocellulaire chez un patient ayant un lichen plan oral et une hépatite C est 125 fois plus élevé.
L’inflammation chronique semble être le facteur essentiel pour le développement du cancer (15-20).
TRAITEMENT
Devant des lésions lichénoïdes, il faut instaurer une hygiène bucco-dentaire parfaite ainsi que le traitement de toutes les maladies générales : maladie hépatique, diabète et hypertension.
Pour les lésions lichénoïdes de contact, il faut opter pour la suppression des irritants locaux (tabac, alcool, surface rugueuse, prothèse mal adaptée et amalgames).
Alors que pour les lésions lichénoïdes d’origine médicamenteuse, des études ont montré que le changement de médicament peut donner de bons résultats après quelque mois.
Dans les cas de lésions lichénoïdes du greffon contre l’hôte, le traitement de 1ère intention est la corticothérapie locale associée à une corticothérapie générale. En 2ème intention, on peut prescrire un inhibiteur de la calcineurine (la ciclosporine et le tacrolimus) en application locale associé parfois à un traitement systémique.
LPB (21, 12)
Les mesures précédentes s’imposent mais sont insuffisantes. Des traitements spécifiques doivent être mis en œuvre.
Pour les LP symptomatiques, la corticothérapie locale est utilisée en première intention à base des dermocorticoïdes en crème (Betneval®, Diprosone®), de l’acétonide de triamcinolone en bains de bouche. La prednisolone peut être prescrite en comprimés orodispersibles de 20 à 40 mg dans un 1/2 verre d’eau en bains de bouche deux à trois fois par jour.
Devant des lésions réfractaires à la corticothérapie locale ou bien une persistance de la symptomatologie, l’injection sous-lésionnelle de corticoïde à libération prolongée tel que l’acétonide de triamcinolone (Kénacort retard® : 40mg), 1 à 2ml toutes les deux semaines, donne de bons résultats.
La prednisone (Cortancyl®) est prescrite par voie systémique, en l’absence de contre-indication, à la dose de 1 mg/kg par jour pendant une durée de dix à 15 jours, puis rapidement dégressive sur un à deux mois, avec un éventuel relais par une corticothérapie locale afin d’éviter les récidives à l’arrêt.
D’autres traitements peuvent être utilisés pour le traitement des LPB, mais dont l’efficacité reste discutable. Les rétinoïdes qui ont une action sur les kératinocytes et ils ont un effet anti-inflammatoire et immunomodulateur. D’autres auteurs proposent l’utilisation de la ciclosporineen bains de bouche, ou appliquée au doigt. Le tacrolimus (Fujimycine®) qui est un macrolide immunosuppresseur peut être prescriten bains de boucheou en crème 0,1 %, de 2 à 4 applications/j(22).
CONCLUSION
Devant toute lésion buccale, les lésions cutanées doivent être recherchées et une sérologie Hépatite virale « C » doit être demandée, bien que cette dernière soit actuellement controversée.
Les facteurs irritatifs, tels que le tabac et l’alcool, les épices, la mauvaise hygiène buccodentaire et les matériaux métalliques dentaires sont à supprimer.
Le diagnostic positif repose sur l’interrogatoire, l’examen clinique et anatomo-pathologique.
Le traitement de première intention est un traitement local. En cas d’échec, le traitement systémique s’impose.
La prise en charge du Lichen plan buccal doit tenir compte de la part psychosomatique de la maladie ainsi que du retentissement psychologique de la symptomatologie lié surtout à la forme érosive,douloureuse, chronique, génératrice de stress, dépression et anxiété, eux-mêmes facteurs déclenchant des poussées de la maladie. Un traitement psychotrope type anxiolytique ou antidépresseur est à discuter, éventuellement associé àun suivi psychologique.
BIBLIOGRAPHIE
2. Chbicheb S., EL WadyW. Lichen plan buccal.EMC Stomatologie. 22-050-0-10,2008.
3. Cendras J., Bonnetblanc J.-M..Erosive oral lichenplanus.Annales de dermatologie et de vénéréologie, 2009, 136, 458—468
4. Otsmane F., Ammar-Khodja A., Benkaidali Ii. Lichen et infection par le virus de l’hépatite C. Ann DermatolVenereol, 2005, 132:9S271-9S279
5. Nita Chainani-Wu.Hepatitis C virus and lichen planus: A review. Oral Surg Oral Med Oral Pathol Oral RadiolEndod, 2004,98 171-183
6. Harden D., Skelton H., Smith KJ. Lichen planus associated with hepatitis C virus: no viral transcripts are found in the lichen planus, and effective therapy for hepatitis C virus does not clear lichen planus. J Am AcadDermatol., 2003, 49(5),847-52.
7. Giuliani M.Lack of association between oral lichen planus and hepatitis c virus infection.Oral Surg Oral Med Oral Pathol Oral RadiolEndod, 2005, 100, 40-51
8. Ghodsi SZ.,DaneshpazhoohM., Shahi M., Nikfarjam A.Lichen planus and Hepatitis C: a case-control study. BMC Dermatology 2004, 4
9. Cheng Y-S.L., Rees T.D. Lichen planuspemphigoides in a hepatitis c patient.Oral And Maxillofacial Pathology, 2003, 96(3), 293
10. Gunning S.T., Turiansky GW. Successive linear, generalized, and oral lichen planus in a patient with chronic hepatitis C infection. J Am AcadDermatol December, 2003, 49(6), 1190-1
11. BenYahya.I.Lichen plan buccalsigneprédictifd’unehépatitevirale « C ». Actualitésodonto-stomatologiques , 2002, 220, 431-440.
12. Al-hashimiI. et Coll. Oral lichenplanus and oral lichenoidlesions: diagnostic and therapeuticconsiderations. Oral Surg Oral Med Oral Pathol Oral RadiolEndod, 2007, 103, e1-12
13. Thornhill M. H., PEMBERTON M. N., SIMMONS R. K., THEAKER E. D.Amalgam-contact hypersensitivity lesions and oral lichen planus. Oral Surg Oral Med Oral Pathol Oral Radiol Endod.,2003, 95(3), 291-9
14. Yumiko N..Histopathological and immunohistochemical study of oral lichen planus-associated HCV infection. European Journal of Internal Medicine, 2000,11, 277–282
15. Bermejo-Fenoll A., Sanchez-Siles M., López-Jornet P., Camacho-Alonso F., Salazar-Sanchez N.Premalignant nature of oral lichen planus. A retrospective study of 550 oral lichen planus patients from south-eastern Spain. Oral Oncology,2009, 45, (e54-6)
16. Fatahzadeh M., Rinaggio J., ChiodoT.Squamous cell carcinoma arising in an oral lichenoid lesion. J Am DentAssoc., 2004, 135, 754-9
17. Stella Lysitsa. Lichen plan buccal : histoire naturelle et transformation maligne. Med BuccaleChirBuccale, 2007, 13, 19-29
18. G. Abbate. Neoplastic transformation of oral lichen: case report and review of the literature. Acta OtorhinoLaryngolItal2006, 26, 47-52
19. L. Ben Slama. Affections potentiellement malignes de la muqueuse buccale : nomenclature et classifictaion. Rev. Stomatol. Chir. Maxillofac, 2010 , 111(4), 208-212
20. Gandolfo S et coll. Risk of oral squamous cell carcinoma in 402 patients with oral lichen planus: a follow-up study in an Italian population. Oral Oncol, 2004, 40, 77-83.
21. David F. Pathophysiology, Etiologic factors, and clinical management of oral lichen planus, part I: facts and controversies. Clinics in Dermatology, 2010, 28, 100–108
22. RianoArguelles A., Martino Gorbea R., Iglesias Zamora M.E., GarateaCrelgo J.Topic tacrolimus, alternative treatment for oral erosive lichen planus resistant to steroids: A case report. Med Oral Patol Oral Cir Bucal, 2006, 11(6), E462-6.








