M. ELFAROUKI*, N. KHLIL*, I. BENKIRANE**, J. KISSA*
* : Service de parodontologie de CHU de Casablanca.
**: Service d’odontologie conservatrice, CHU de Casablanca.
Faculté de médecine dentaire de Casablanca - Maroc
Université Hassan II
RÉSUMÉ
Les lésions endo-parodontales combinées ou vraies sont le résultat de la coexistence d’une lésion d’origine endodontique et une autre d’origine parodontale sur la même dent. Elles apparaissent habituellement dans un contexte de parodontite généralisée.
La lésion liée à la nécrose pulpaire et celle en rapport avec une maladie parodontale évoluent indépendamment l’une de l’autre et de façon parallèle. Leurs évolutions aux dépens des structures parodontales est telle qu’elles finissent par se rencontrer et fusionner formant ainsi une seule lésion qu’on appelle lésion endo-parodontale vraie (1).
Le but de cet article est d’illustrer la démarche diagnostique et thérapeutique pouvant être adoptée par le chirurgien dentiste devant une telle lésion , et ce, à travers un cas clinique.
Les dents et le parodonte constituent une véritable unité anatomophysiologique, et ce grâce aux différentes voies de communications qu’ils entretiennent. Ces communications permettent à la pulpe et au parodonte d’entretenir des rapports vasculaires, nerveux et sensoriels (1, 2).
Si la région péri- apicale est le lieu privilégié de communication entre la pulpe et le parodonte, il ne faut pas ignorer le rôle des canaux radiculaires accessoires et des tubulis dentinaires dans les échanges pulpo-parodontaux.
En plus de ces voies de communication physiologiques, d’autres communications peuvent s’installer soit après progression d’une pathologie endodontique ou parodontale, soit de manière iatrogène ou traumatique (Perforations radiculaires, résorptions radiculaires internes ou externes, fractures radiculaires) (1,3).
Toutes ces communications favorisent la transmission réciproque des phénomènes inflammatoires et dégénératifs (3).
Les lésions endo-parodontales combinées ou mixtes sont le résultat de la coexistence d’une lésion d’origine endodontique et une autre d’origine parodontale sur la même dent. Elles apparaissent habituellement dans un contexte de parodontite généralisée (3,4).
La lésion liée à la nécrose pulpaire et celle en rapport avec une maladie parodontale évoluent indépendamment l’une de l’autre et de façon parallèle. Leurs évolutions aux dépens des structures parodontales sont telles qu’elles finissent par se rencontrer et fusionner formant ainsi une seule lésion appelée lésion endo-parodontale vraie, appelée encore lésion endo-parodontale combinée (3).
En effet, l’évolution de la maladie parodontale entraîne la migration de l’attache épithélio-conjonctive dont la profondeur est différente d’un site à l’autre sur la même dent, d’où un sondage parodontal arciforme ; alors que la lésion endodontique cherche à s’extérioriser dans le milieu buccal grâce à une fistulisation en suivant le chemin de moindre résistance qui n’est autre que la fistule desmodontale donnant un sondage punctiforme (Harrington) (3,5).
Du fait de la combinaison étiopathogénique, l’aspect microbiologique des lésions endo-parodontales combinées reflète celui des lésions endodontiques d’une part et parodontales d’autre part (Rotstein et Simon, 2004) (6).
DÉMARCHE DIAGNOSTIQUE
Le diagnostic positif des lésions endo parodontales vraies repose sur Les données de l’examen clinique, à savoir le degré d’évolution et la sévérité de la maladie parodontale d’une façon globale, et sur l’état endodontique et parodontal de la dent en question (3, 6, 7).
La difficulté que peut rencontrer le praticien réside surtout dans la détermination de l’origine exacte de ces lésions dont dépend la stratégie thérapeutique.
Souvent le patient consulte en urgence rapportant à la fois des signes en faveur de la parodontite péri apicale et des signes en faveur de l’abcès parodontal, avec des douleurs pulsatiles associées à une sensation de dent longue, localisées sur une dent ou irradiante sur tout un secteur.
Sur la dent en question, l’examen clinique révèle la présence d’une tuméfaction gingivale avec ou sans fistule, le degré de mobilité est variable.
Le test de sensibilité pulpaire est négatif relevant une nécrose pulpaire. La communication endo parodontale peut être matérialisée en passant une sonde parodontale au niveau du sillon gingivo dentaire, l’enfouissement brusque et punctiforme de la sonde reflète la voie de communication (3).
Le cliché rétro alvéolaire met en évidence deux zones radioclaires coniques opposées par leur sommets : la lésion parodontale a un sommet en apical, alors que la lésion endodontique a un sommet cervical (3).
La continuité entre la poche parodontale et la lésion d’origine endodontique peut être individualisée grâce à une radiographie rétro alvéolaire cône de gutta en place.
Le diagnostic différentiel permet de faire la distinction entre (8, 9, 10) :
• Lésion endo parodontale d’origine endodontique,
• Lésion endo parodontale d’origine parodontale,
• Lésion endo parodontale vraie combinée.
Le tableau (1) montre les éléments du diagnostic différentiel (3,8).
| Test de sensibilité pulpaire |
Sondage parodontal |
Radiographie | Contexte général |
|
| Lésion d'origine endodontique |
Négatif | Punctiforme | Elargissement desmodontale ou endo parodontale |
Dent non concernée par la maladie parodontale |
| Lésion d'origine parodontale |
Positif | Cironférentiel en U |
Lyse osseuse dépendante du type de la parodontite |
Parodontite |
| Lésion endo parodontale vraie |
Négatif | Circonférentiel en V |
Radioclarté sous forme de 2 cônes opposées + lyse osseuse pathognomonique de lamaladie parodontale |
Parodontite |
CAS CLINIQUE :
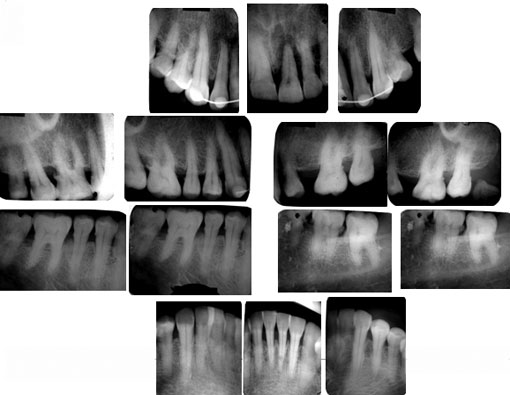

Madame B.F, âgée de 56 ans, est venue consulter en urgence pour une tuméfaction gingivale, purulente, douloureuse, pulsatile, et diffuse en regard de la 21 qui présente également une mobilité accrue.
L’examen clinique et radiologique montre que la patiente présente une parodontite chronique généralisé (AAP, 1999) (fig 1 et 2).
Le tableau suivant montre la conclusion de la démarche diagnostique sur la 21 (tableau 2).
A la lumière des données cliniques on en conclut qu’il s’agit d’une lésion endo parodontale vraie.
L’origine de la lésion est mixte, endodontique et parodontale ; l’origine parodontale est évidente vu l’atteinte parodontale généralisée sur la plupart des dents, alors que l’origine de la nécrose pulpaire est mal comprise, elle est attribuée à la présence de la fêlure sur la face vestibulaire.
| Aspect clinique |
Sensibilité pulpaire |
Sontage parodontal |
Mobilité | Radiographie | |
| Dent 21 |
Félure coronaire Dyschromie |
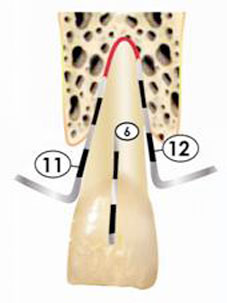
Négatif | Sondage en "V" selon Harrington (11) (fig 3) |
Degré 4 selon Muhleman |
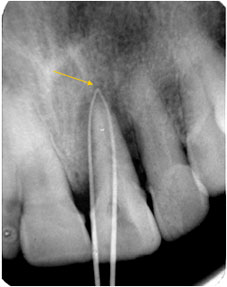
Image en deux cônes opposés par leur sommets en place montre une communication endo parodontale (fig 4) |
 |
 |
DÉMARCHE THÉRAPEUTIQUE
L’objectif du traitement consiste dans un premier lieu en la désinfection du système canalaire, suivie par le débridement parodontal en second lieu, pour induire les conditions favorables à la cicatrisation.
Après cette phase thérapeutique, le patient sera soumis à un contrôle régulier (sondage, radiographie..) lors de la phase de réévaluation et durant la phase de maintenance (7,12, 13, 14).
En urgence, notre but essentiel était de soulager la patiente et d’éviter les conditions qui peuvent déclencher la douleur.
Nous avons procédé en premier lieu à la création d’une voie de drainage canalaire en réalisant une large cavité d’accès. Le drainage canalaire a été obtenu progressivement grâce au passage de limes dans le système canalaire sous irrigation abondante à l’hypochlorite de sodium.
Après assèchement du canal, une obturation canalaire à l’hydroxyde du calcium a été réalisée.
Vu la mobilité excessive de la 11 et pour éviter tout traumatisme occlusal, une contention semi rigide de 13 à 23 a été réalisée.
Le drainage de l’abcès parodontal a été fait grâce au détartrage supra et sous gingivale.
Grace à ces manœuvres simples, nous avons pu obtenir un soulagement immédiat.
En fin de cette première séance, une antibiothérapie à base de spiramycine et métronidazole (birodogyl*) a été prescrite.
Après 15 jours, le traitement parodontal proprement dit a été accompli (détartrage et surfaçage maxillaire et mandibulaire) selon le principe de désinfection globale de la cavité buccale en une seule séance.
Après deux mois, le contrôle clinique et radiologique a montré une nette amélioration avec réduction de l’inflammation gingivale, absence de douleur, et la réduction de la mobilité dentaire.
Dans ces conditions bien précises, nous avons opté pour l’obturation canalaire définitive à la gutta percha.
Les visites de contrôle régulier ont été programmées durant la phase de réévaluation et puis durant la phase de maintenance.
Le schéma suivant illustre la démarche thérapeutique (fig 5 ) :
|
J0
|
traitement d’urgence
Détartrage Désinfection canalaire et obturation à l’hydroxyde de calcium Obturation coronaire hermétique Surfaçage de la 21 Contention semi rigide de 13 à 23 Antibiothérapie + Bain de bouche 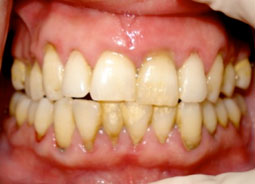 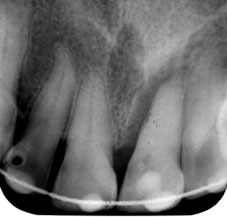 J0: traitement d’urgence
|
|
J15
|
Traitement parodontal proprement dit : surfaçage maxillaire et mandibulaire
|
|
2 mois
|
Contrôle clinique et radiologique→ stabilité→ obturation canalaire définitive à la Gutta percha
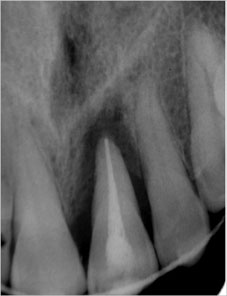 2 mois: obturation canalaire définitive |
|
4 mois
|
Réévaluation:
Amélioration de la profondeur des poches généralisée + absence de douleur+ absence de saignement au sondage+ signe radiologiques de minéralisation osseuse  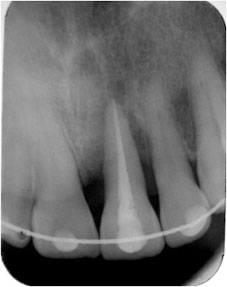 Après 4 mois: régénération osseuse tout autour de la 21
|
| 12 mois |
Maintenance parodontale :
dépose de contention contrôle clinique et radiologique→ gain osseux 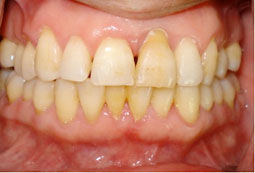 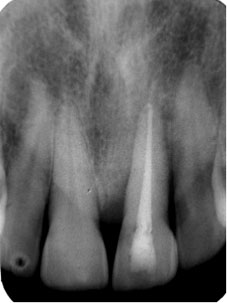 Après 12 mois: dépose de la contention, on note une stabilité parodontale avec une régénération osseuse presque ad intégrum |
Du fait de l’origine combinée des lésions endo-parodontales vraies, le traitement requiert un traitement endodontique au départ suivi d’un traitement parodontal approprié, et ce pour les raisons suivantes (12):
• Il a été montré que l’infection endo-canalaire favorise la migration apicale de l’épithélium de jonction le long de la surface dentinaire dénudée (15).
• La présence de bactéries dans le canal affecte le résultat du traitement parodontal (3) .
• Les défauts parodontaux induits expérimentalement au niveau des dents avec pulpe infectée montrent une aggravation de la migration apicale de l’épithélium d’une valeur de 20% plus que les dents non infectées (16).
• La désinfection canalaire suivie d’une obturation hermétique favorise la cicatrisation péri apicale (3).
L’hydroxyde de calcium est un agent anti-bactérien très puissant. Grâce à son PH élevé il peut entraîner la destruction de plus de 99.9% des bactéries en moins de 6 minutes, comme il peut favoriser l’activité cicatricielle des tissus périapicaux.
L’ obturation définitive à la gutta percha ne sera réalisée qu’en présence d’un silence clinique.
L’obturation à la gutta percha va se comporter comme une véritable suture endodontique qui a pour but de sceller le maximum des voies de communication endo-parodontale (3, 7).
Le traitement et le pronostic parodontal sont conditionnés par le résultat obtenu après traitement endodontique.
Enfin, le pronostic des lésions endo-parodontales vraies dépend (3):
• De l’ancienneté de la lésion,
• Du diagnostic et de la chronologie des étapes thérapeutiques et de la qualité de la prise en charge,
• Et surtout du degré de la participation endodontique.
Lorsque la lésion endo-parodontale est ancienne, on se retrouve devant un écosystème bien adapté qui favorise plus de résistance à la thérapeutique adoptée.
Selon Bergenholtz et Hasselgren, dans les cas de lésion endo-parodontale vraie, le pronostic de régénération de l’appareil d’attache dépend surtout du pronostic endodontique (17).
En conclusion, Le taux de succès que nous pouvons obtenir est tributaire :
• De la précision du diagnostique grâce aux différents outils diagnostic,
• De la rapidité de la prise en charge,
• De la maitrise des facteurs de risque,
• Du degré de motivation et de la patience du patient.
En fin, nous précisons qu’une attention bien particulière doit être faite quant au rôle de la maintenance parodontale dans l’entretien des résultats à long terme.
BIBLIOGRAPHIE
1- H. RANGÉ, Les relations complexes entre parodonte et endodonte. Rev Odont Stomat 2007;36:161-178
2- PV. ABBOTT, Classification, diagnosis and clinical manifestations of apical periodontitis. Endodontic Topics 2004, 8, 36–54
3- Sartori S, Silvestri M, Cattaneo V. Endoperiodontal lesion. J Clin Periodontol 2002; 29: 781–783. CBlackwell Munksgaard, 2002.
4- S. Lin, G. Tillinger, O. Zuckerman. Endodontic-periodontic Bifurcation Lesions: A Novel Treatment Option. The Journal of Contemporary Dental Practice, Volume 9, No. 4, May 1, 2008
5- Dongari A, Lambrianidis T. Periodontally derived pulpal lesions. Endod Dent Traumatol 1988; 4: 49-54.
6- ROTSTEIN I, SIMON J. Diagnosis, prognosis and decision-making in the treatment of combined periodontal-endodontic lesions. Periodontol 2000 2004;34:165-203.
7- H. Haueisen & D. Heidemann. Hemisectionfor treatmentof an advanced endodontic-periodontal lesion: a casereport. Int Endodontic Journal, 35, 557-572, 2002
8- Zehnder M, Gold SI, Hasselgren G. Pathologic interactions in pulpal and periodontal tissues. J Clin Periodontol 2002; 29: 663–671.
9- Gary C. Armitage. Development of a Classification System for Periodontal Diseases and Conditions. Ann Periodontol. Volume 4 • N° 1 • December 1999
10- ROTSTEIN I, SIMON J. The endo-perio lesion: a critical appraisal of the disease condition. Endodontic Topics 2006, 13, 34–56
11- HARRINGTON GW, STEINER DR, AMMONS WF. The periodontal-endodontic controversy. Periodontol 2000 2002; 30:123-130.
12- Chen S- Y. Wang H-L. Glictkman GN: The influence of endodontic treatment upon periodontal wound heating. J Clin Periodontol 1997: 24: 449—456
13- P. H. A. GULDENER, The relationship between periodontal and pulpal disease. International Endodontic Journal (1985) 18,41-54
14- S B. Blanchard, A. Almasri, J. L. Gray. Periodontal-Endodontic Lesion of a Three-Rooted Maxillary Premolar: Report of a Case. J Periodontol • May 2010
15- Blomlof, L., Lengheden, A. & Lindskog, S. (i992) Endodontic infection and caicium hydroxide-treatment. Effects on periodontai heaiing in mature and immature replanted monkey teeth. Journal of Clinical Periodontol 19, 652-658
16- Jansson. L., Bhnevid, H., Blomlof, L., Weintraub, A. & Lindskog, S. (1995) Endodontic pathogens in periodontal disease augmentation. Journal of Clinical Periodontol 22, 598-602.
17- BERGENHOLTZ G, HASSELGREN G. Endodontics and periodontics. In : Lindhe J, Karring T, Lang NP, ed. Clinical periodontol and implant dentistry. 3rd ed. Copenhagen : Munksgaard 1997;318-351.








